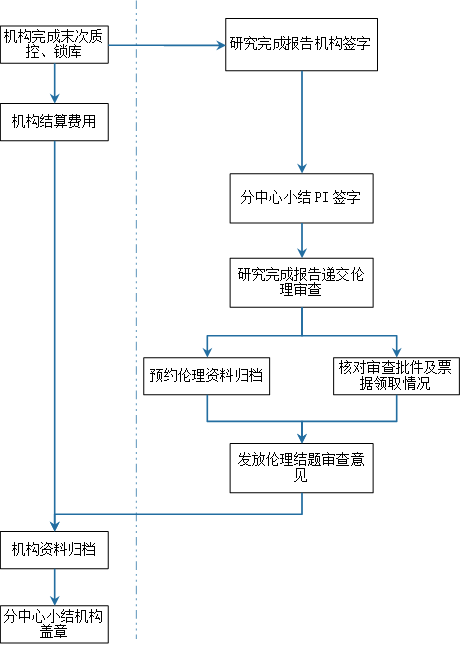
完成临床研究,应及时向伦理委员会提交“研究完成报告”←点击文件名下载,并与伦理办公室预约归档资料,整理“项目资料归档目录”←点击文件名下载。研究完成报告中应明确目前受试者的补偿及赔偿是否均已落实,且获得研究管理部门审核确认。研究完成报告所附分中心小结(如有),应由主要研究者签字确认。
注1:伦理资料归档时间为每周五全天,有需求项目的CRA请提前预约。
注2:试验总结报告需递交伦理备案。
注3:研究完成报告受理后伦理委员会原则上将不再接收任何递交材料(备案材料除外)。
文件递交注意事项:
1. 请先在CTMS系统中填写申请并上传文件,上传文件如需盖章请上传盖章版pdf扫描件,文件如需签字请上传签字件pdf扫描件。如文件有对应的版本及日期,必须在系统中填写完整正确,以免审查意见中产生错误。
2. 请关注CTMS系统进程,形式审查退回后请按要求修改,形式审查通过后请打印受理通知,并尽快将1份纸质材料递交伦理办公室,纸质材料接收后进入正式审查流程。如在系统受理后两周仍未递交纸质资料,该文件将在系统上作退回处理。
3. 纸质材料请附系统导出的文件清单,文件的内容、名称、版本与日期必须与CTMS系统中对应一致,安排审查以纸质材料签收时间为准。
4. 伦理递交信中建议以系统导出的文件清单直接作为文件目录,否则请保证文件名称、版本及日期与实际递交文件的一致性。